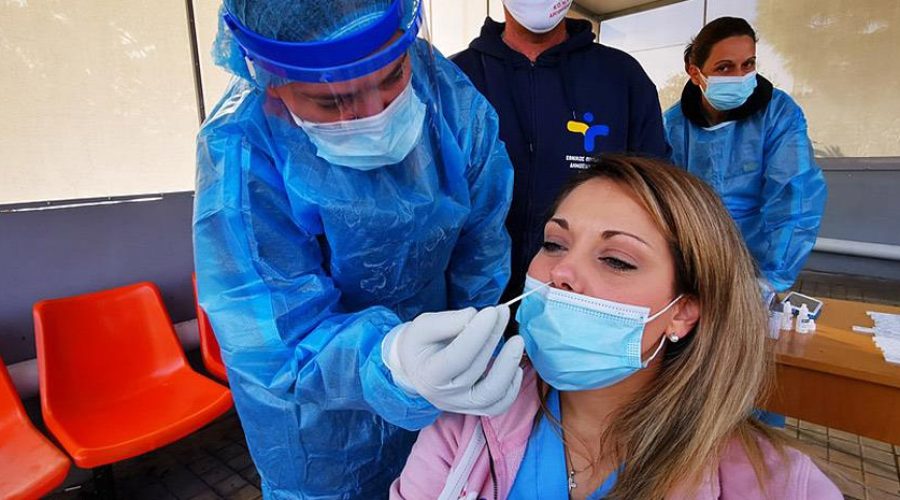
Κορωνοϊός: 572.000 rapid test ζητούν δύο Υγειονομικές Περιφέρειες
Σύμφωνα λοιπόν με ασφαλείς πληροφορίες, μόλις πριν μερικές μέρες η 1η ΥΠΕ και η 2η ΥΠΕ εξέδωσαν προσκλήσεις ενδιαφερομένων που θέλουν να αναλάβουν την προμήθειά τους σε rapid test. Συνολικά μιλάμε για 572.000 τεστ, με την αποσφράγιση των προσφορών να γίνεται εντός των προσεχών ημερών.
Τι ζητά η 1η Υ.ΠΕ (Υγειονομική Περιφέρεια)
Την επείγουσα προμήθειά της σε 300.000 ιατροτεχνολογικά προϊόντα ταχέων ελέγχων αντιγόνων SARS-CoV-2 (rapid test), με κριτήριο ανάθεσης την πλέον συμφέρουσα από οικονομική άποψη προσφορά για την κάλυψη των αναγκών στα Νοσοκομεία και των Δομών Π.Φ.Υ που καλύπτει.
Τι ζητά η 2η Υ.ΠΕ (Υγειονομική Περιφέρεια)
Ζητά την κατεπείγουσα προμήθειά της σε 272.100 τεμάχια ιατροτεχνολογικών προϊόντων ταχέων ελέγχων αντιγόνων SARS-CoV-2 (rapid test).
Στη μεν 1η Υ.ΠΕ η αποσφράγιση των προσφορών έχει δρομολογηθεί στις 4/3/2022, ενώ στην 2η ΥΠΕ στις 8/3/2022. Και στις δύο περιπτώσεις πάντως έχει οριστεί ότι η παράδοση θα γίνεται τμηματικά και ειδικότερα: το 30% της συνολικής ποσότητας, θα παραδοθεί σε διάστημα ενός (1) μήνα, το 40% της ποσότητας το δεύτερο μήνα και το 30%της ποσότητας τον τρίτο μήνα (από την υπογραφή της σύμβασης).
Ποια χαρακτηριστικά απαιτείται να έχουν τα rapid test
- να ανιχνεύουν αντιγόνο του SARS–CoV–2,
- να εκτελούνται σε δείγματα ρινικά, φαρυγγικά ή ρινοφαρυγγικά ή σε δείγμα σάλιου,
- να έχουν έγκριση CE–IVD, η έγκριση FDA–EUA είναι επιθυμητή αλλά όχι υποχρεωτική,
- να βγάζουν αποτέλεσμα εντός τριάντα (30) λεπτών,
- να είναι επιδεκτικά μακροχρόνιας φύλαξής τους (πλέον του 1 μήνα) σε συνθήκες θερμοκρασίας δωματίου (5 με 30 βαθμοί Κελσίου),
- η εκτέλεση και η ολοκλήρωση του test να γίνεται αποκλειστικά με εξοπλισμό που διατίθεται στο kit, ώστε να μπορεί το test να διατεθεί και να γίνεται οπτική ανάγνωση των αποτελεσμάτων χωρίς συνοδό εξοπλισμό ταυτόχρονα σε πολλαπλές περιοχές στην Ελλάδα,
- να μπορούν να εκτελεστούν συγχρόνως και ανεξάρτητα πολλαπλά δείγματα,
- να είναι εύκολα στη χρήση τους στη λογική των Point of Care Test, ώστε να μην απαιτείται προσωπικό εξειδικευμένο σε πειράματα/εξετάσεις μοριακής βιολογίας, αλλά να μπορεί να εκτελεστεί από υγειονομικό προσωπικό (όπως ιατροί, νοσηλευτικό προσωπικό).
Η ευαισθησία της δοκιμασίας για ανίχνευση SARS–CoV–2, όπως αυτή προκύπτει από την επαρκή αξιολόγηση (WHO, FIND ), πρέπει να είναι ίση η μεγαλύτερη από 85% (μέση ή διάμεση τιμή) σε δείγματα που έχουν βγει με realtime PCR. Η ειδικότητα της δοκιμασίας για ανίχνευση SARS–CoV–2 θα πρέπει να είναι ίση ή μεγαλύτερη από 98% (μέση ή διάμεση τιμή) σε δείγματα που έχουν βγει αρνητικά με realtime PCR.
YgeiaOnline ,το πρώτο Portal Υγείας. Βρείτε γιατρούς, νοσοκομεία, φαρμακεία και ότι έχει να κάνει με την υγεία. Κλείστε ηλεκτρονικά ραντεβού με γιατρούς, απομακρυσμένη διάγνωση και πολλές άλλες υπηρεσίες που μόνο το YgeiaOnline.gr μπορεί να προσφέρει.